Reactivo IgG MO22196para western blotpara inmunofluorescenciapara inmunocitoquímica
Añadir a mis favoritos
Añadir al comparador
¿Quiere comprar directamente?
Visite nuestra Shop.
Características
- Tipo
- IgG
- Aplicaciones
- para western blot, para inmunofluorescencia, para inmunocitoquímica
- Formato
- líquido
- Marcador probado
- PEA15
- Origen
- del ratón
- Temperatura de almacenamiento
Máx.: 4 °C
(39 °F)Mín.: -20 °C
(-4 °F)
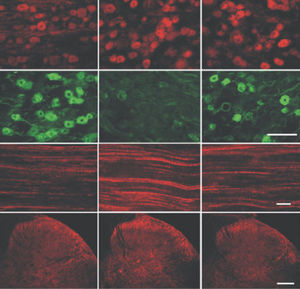
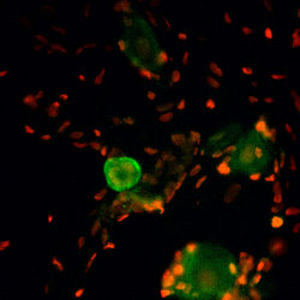
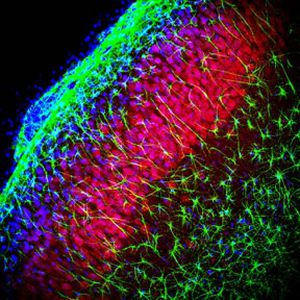
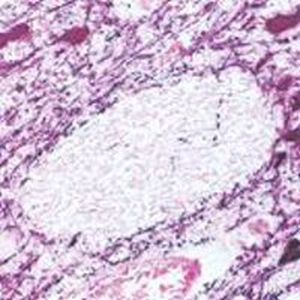
Descripción
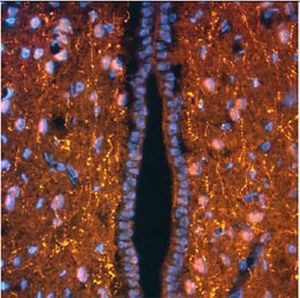
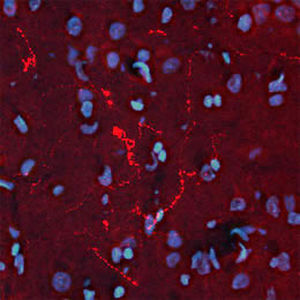
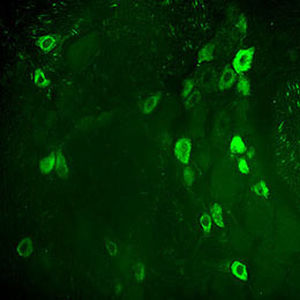
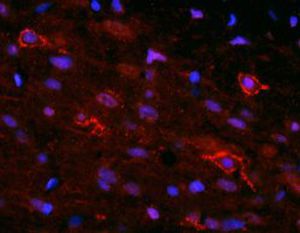
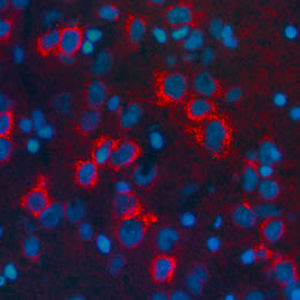
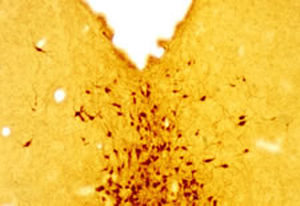
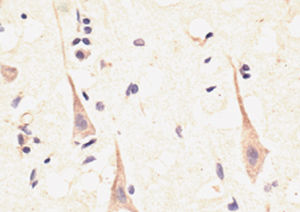
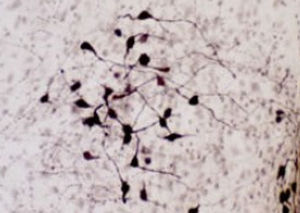
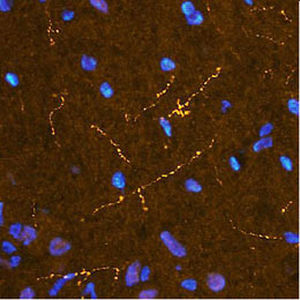
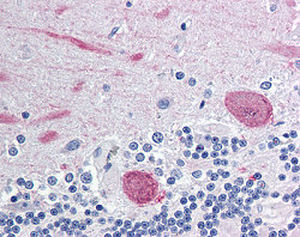
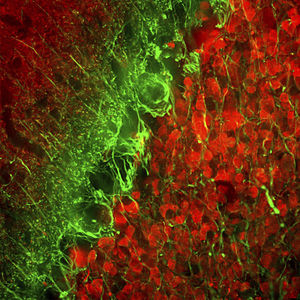
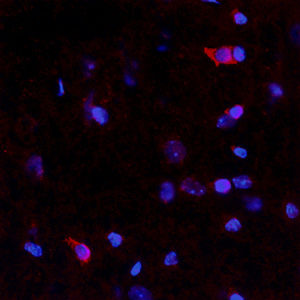
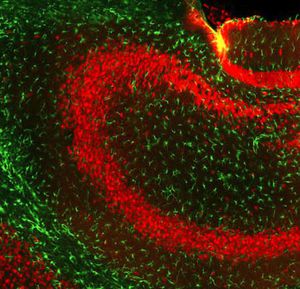
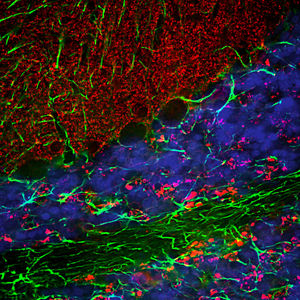
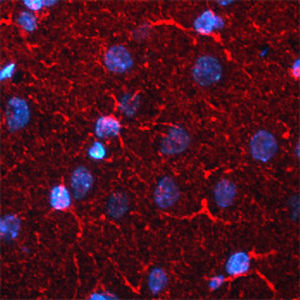
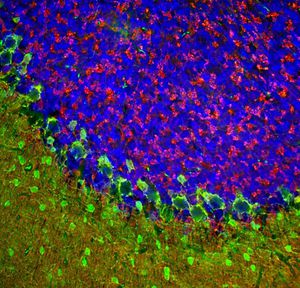
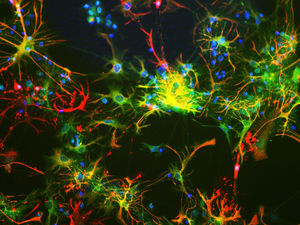
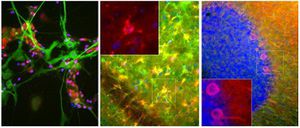
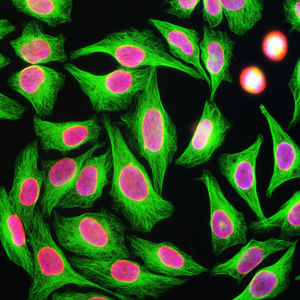
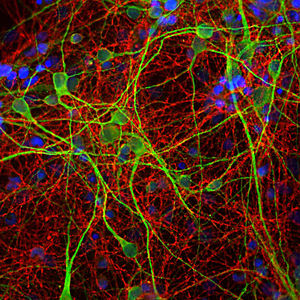
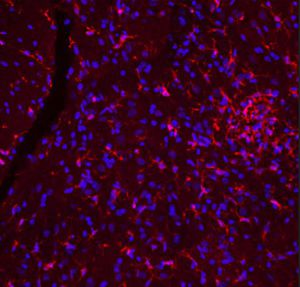
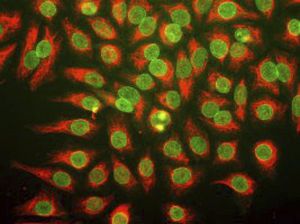
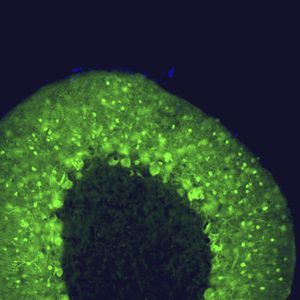
La PEA-15 se aisló originalmente como una proteína principal de bajo peso molecular de astrocitos estriatales embrionarios de ratón cultivados en células. Se demostró que tres manchas en geles 2D con un peso molecular aparente de 15kDa y un punto isoeléctrico de 5,1-5,3 eran formas diferentes de una proteína. La proteína fue serina fosforilada en un sitio por la proteína quinasa C tanto in vivo como in vitro y la proteína fue llamada "fosfoproteína enriquecida en astrocitos de 15kDa", de ahí PEA-15. La clonación y secuenciación posteriores revelaron que se trataba de una proteína con una secuencia bien conservada entre el ratón y el ser humano y que se expresaba en gran medida en el cerebro. De forma independiente, se descubrió que la misma proteína estaba regulada al alza en fibroblastos y tejidos de pacientes diabéticos, por lo que se denominó "proteína enriquecida en diabetes" o PED. Estudios inmunocitoquímicos demostraron que la proteína se expresaba en gran medida en astrocitos y ciertas neuronas del SNC de ratones, aunque se expresa a niveles más bajos de forma ubicua. Se demostró que la PEA-15 interacciona con la quinasa regulada por señales extracelulares y regula la entrada nuclear de esta proteína, y se han descrito varias otras interacciones importantes con otras proteínas implicadas en la regulación de la apoptosis, el metabolismo de la glucosa y el crecimiento celular. El MCA-4D2 se fabricó contra una construcción recombinante de PEA-15 de longitud completa expresada y purificada a partir de E. coli.
---
Catálogos
No hay ningún catálogo disponible para este producto.
Ver todos los catálogos de NeuromicsBúsquedas asociadas
- Kit de reactivos
- Kit de reactivos para biología molecular
- Kit de reactivos líquido
- Kit de reactivos para la investigación
- Software de análisis
- Kit de reactivos de proteínas
- Reactivo por inmunología
- Kit de reactivos anticuerpos
- Software de laboratorio
- Kit de reactivos liofilizado
- Kit de reactivos de suero
- Kit de reactivos para inmunohistoquímica
- Kit de reactivos para enzimas
- Reactivo para la investigación científica
- Kit de reactivos anticuerpo monoclonal
- Kit de reactivos para western blot
- Software para la investigación
- Reactivo para inmunofluorescencia
- Kit de reactivos citoquina
- Reactivo anticuerpo policlonal
* Los precios no incluyen impuestos, gastos de entrega ni derechos de exportación. Tampoco incluyen gastos de instalación o de puesta en marcha. Los precios se dan a título indicativo y pueden cambiar en función del país, del coste de las materias primas y de los tipos de cambio.